-

快速获得美国FDA医疗器械唯一标识(UDI)的十个步骤
查看详情 2020-10-09 -

FDA:自2020年10月1日起,食品企业需有唯一企业识别码(UFIs)或DUNS编码
查看详情 2020-09-30 -
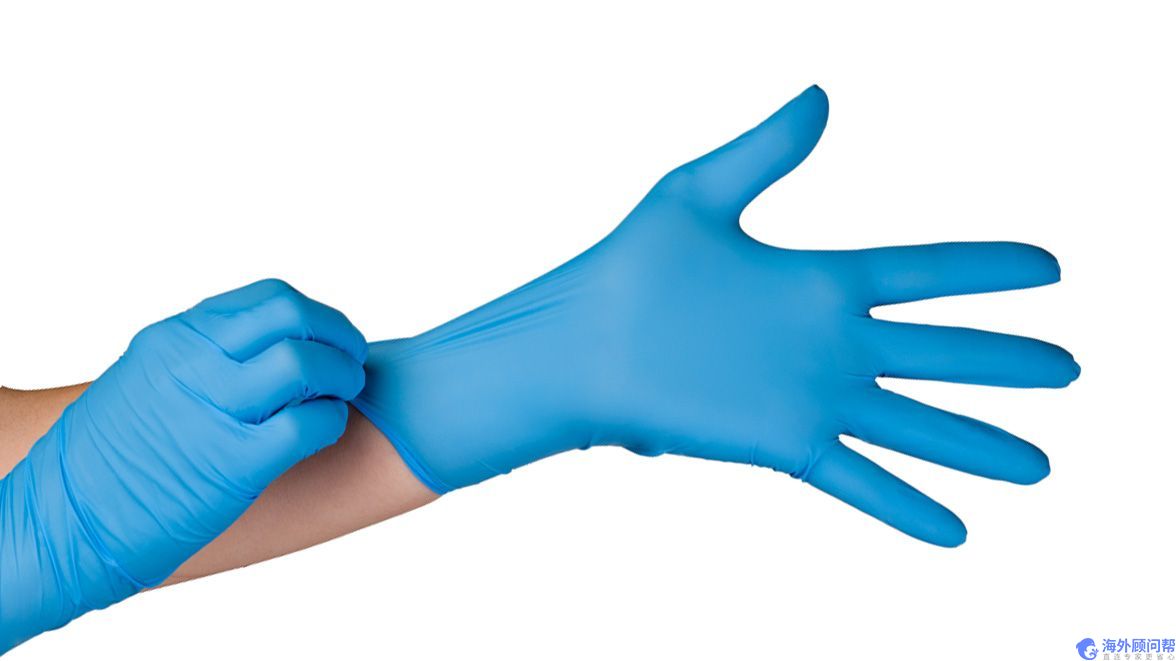
丁腈手套美国的FDA510k申请流程
查看详情 2020-09-30 -

RoHS和REACH对化学品的要求
查看详情 2020-09-29 -
2020年1~6月美国FDA新批准的新型医疗器械简介(下)
查看详情 2020-09-29 -

FDA年费怎么支付?如何支付FDA工厂注册年费?
查看详情 2020-09-29 -

欧盟授权机构是什么意思?
查看详情 2020-09-28 -
欧盟医疗器械法规IVDD和IVDR的区别
查看详情 2020-09-28 -

欧盟医疗器械IVDD产品分类以及认证流程
查看详情 2020-09-28 -
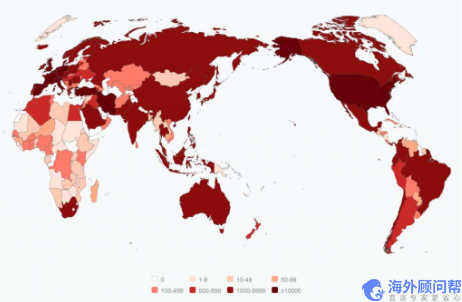
疫情全面反扑!欧洲第二波卷土重来;亚洲新增一路狂飙;美洲确诊持续“霸榜”
查看详情 2020-09-27








