受疫情的影响,美国对于防护用品的需求是非常大的,中国企业如果想把这些产品出口到美国并非易事,除了商务部的白名单,还需要美国的FDA注册。那么,防护服、隔离衣、手术服等防护用品出口美国FDA注册办理流程是什么样的呢?我们一起来看下。

FDA要求所有在美国上市的医疗器械产品都需要进行:
- 设施注册/公司注册(Establishment, Owner/Operator Registration)
- 产品注册/产品列名(MDL: Medical Device Listing)
- 指定FDA注册的美国代理人US Agent
- 涉及到FDA510(K)或PMA监管的产品,还需要先申请510(K)或PMA获批后,才可以进行产品注册
- 如果是从美国境外进口的器械,美国境内进口商还需要单独进行FDA进口商公司注册;与制造商无关
1. 防护服在美国FDA的分类
| 产品类别 | 管理类别 | 产品代码 | 申报方式 | 预期用途 |
| 外科防护服 | 2 | FYC | 510K | 保护病人和医护人员免受微生物、体液和微粒物质的传播 |
| 手术衣 | 2 | FYA | 510K | 保护病人和医护人员免受微生物、体液和微粒物质的传播。一般手术室用 |
| 隔离衣 | 2 | OEA | 510K | 用于医疗机构门诊、病房、检验室等的普通隔离 |
防护服、隔离衣、手术服等防护用品出口美国需要做FDA510K申报。那么,防护服、隔离衣、手术服的FDA510K的办理流程和周期是怎么样的?
2. 防护服、隔离衣、手术服的FDA的办理流程
- 申请人递交510K文件
- 申报受理
- FDA一阶段审核
- 递交发补资料
- FDA二阶段审核
- 通过评审,取得K号
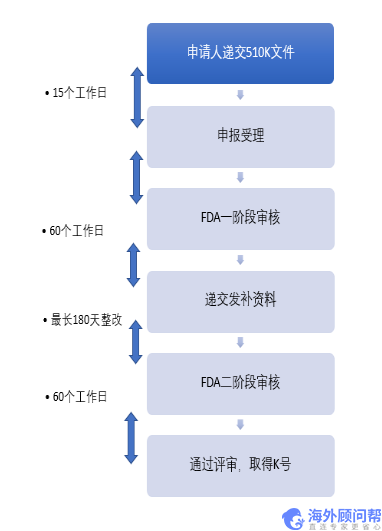
3. 防护服、隔离衣、手术服的FDA的办理周期
按照2类医疗器械的控制方式,递交510K文件至FDA进行评审,取得K号后列名注册。这一系列的过程至少需要6个月的时间。
4. 防护服、隔离衣、手术服做FDA需要做哪些检测?
通常是两个:(1)生物相容性、 (2)产品性能测 。
以上就是关于“防护服、隔离衣、手术服等防护用品出口美国FDA注册办理流程详解!”的相关内容,我们可以为企业提供FDA510K的申报服务,服务内容包括:
1) 依据企业提供产品信息确定产品的代码及分类
2) 根据确定的产品代码寻找对应的注册指南或相关文件,协助企业寻找比对器械,确定产品需要准备的资料和检测项目
3) 在企业准备资料和检测的过程中提供法规技术支持
4) 依据企业提供的相关资料编制510K报告
5) 指导企业向FDA递交小企业资质申请
6) 向FDA申请付款编码,指导企业安排美金支付
7) 递交510K报告至FDA进行评审,负责与FDA联络沟通,并指导协助企业进行整改,直至项目评审结束
【海外顾问帮】是协助国内企业和个人跨境发展一站式的服务中心,协同全球专家顾问,坚持透明服务,打破跨境壁垒,为FDA认证提供一站式服务,咨询电话: 400-106-2206。














