-
什么是欧盟医疗器械MDR法规
查看详情 2021-02-03 -
如何做好IVDD到IVDR更改的准备工作?
查看详情 2021-02-02 -
体外诊断医疗器材(IVDD98/79/EC)指南
查看详情 2021-02-02 -

无线电设备指令(RED)要求的符合性声明都有哪些?
查看详情 2021-02-02 -

欧盟MDD指令与MDR的区别
查看详情 2021-02-02 -

REACH认证和ROHS的区别
查看详情 2021-02-01 -
体外诊断试剂厂商应如何准备IVDR要求?
查看详情 2021-02-01 -
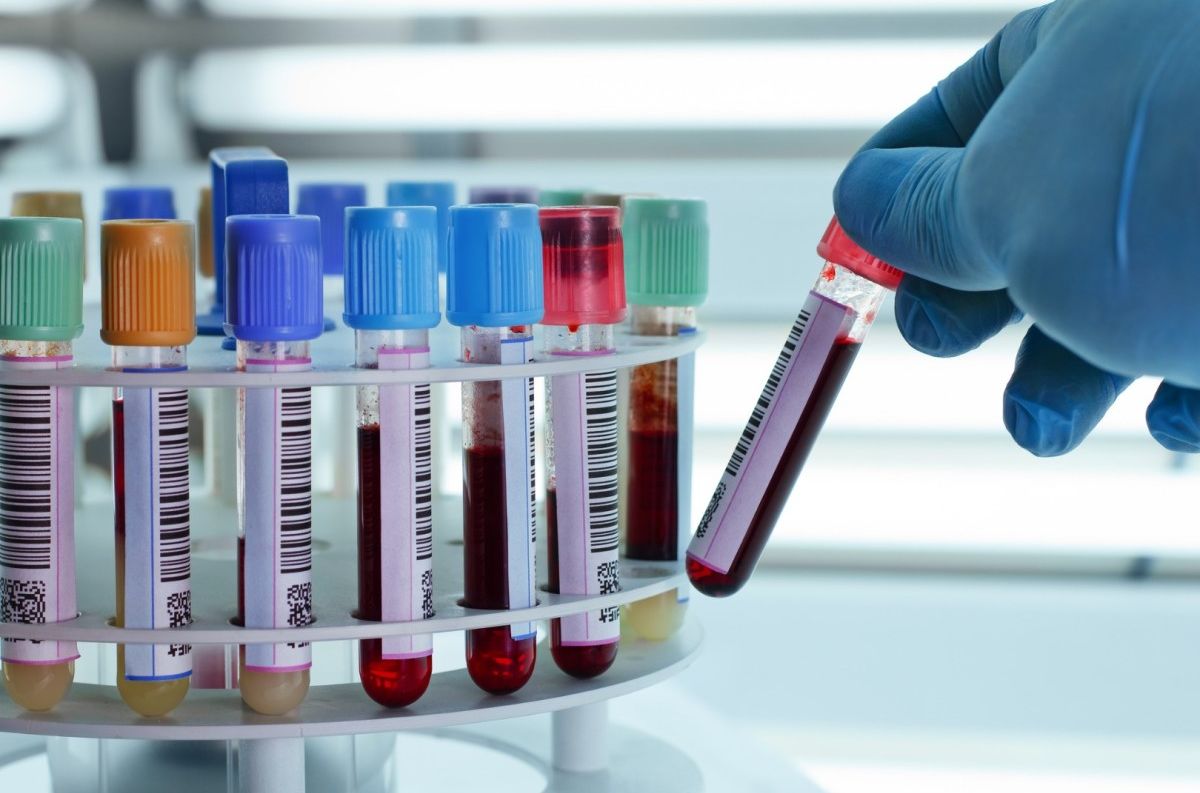
体外诊断试剂器械IVDD申请CE认证和IVDR申请CE认证流程指南
查看详情 2021-02-01 -
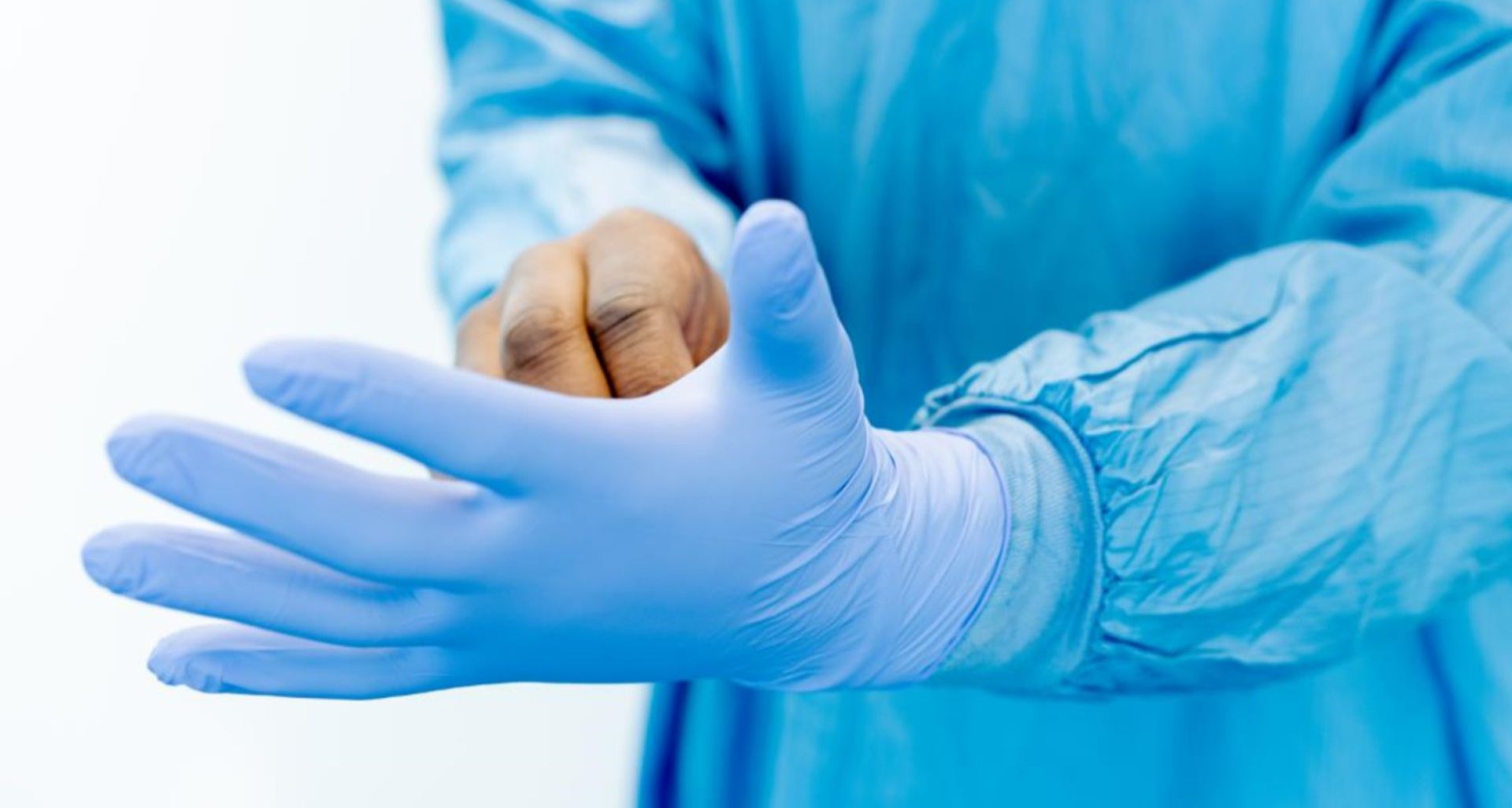
丁腈手套/一次性医用手套/乳胶手套CE认证需要符合欧盟什么标准?
查看详情 2021-01-30 -
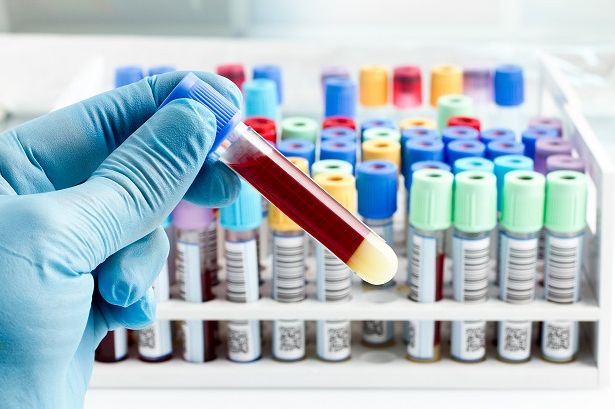
IVDR技术文档内容及要求
查看详情 2021-01-29









