-
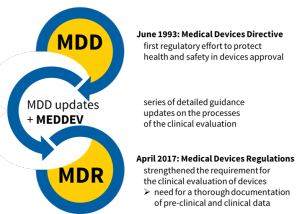
2017年的《医疗器械条例》(MDR)增加了对临床数据记录以支持许可证申请的要求
查看详情 2021-01-29 -

RoHS认证什么意思?
查看详情 2021-01-29 -
欧盟指令MDD和MDR的主要差异
查看详情 2021-01-28 -

ROHS认证有效期多久?
查看详情 2021-01-28 -

MDD向MDR转换需要做哪些工作?
查看详情 2021-01-27 -

福利来了!亚马逊符合性声明DoC(EC Declaration of Conformity)全面指南
查看详情 2021-01-27 -

欧盟CE指令MDD和MDR的区别有哪些?
查看详情 2021-01-27 -

MDD指令CE技术文件清单
查看详情 2021-01-27 -

FDA验厂需要准备什么?
查看详情 2021-01-27 -

医疗器械MDD指令适用范围
查看详情 2021-01-26









