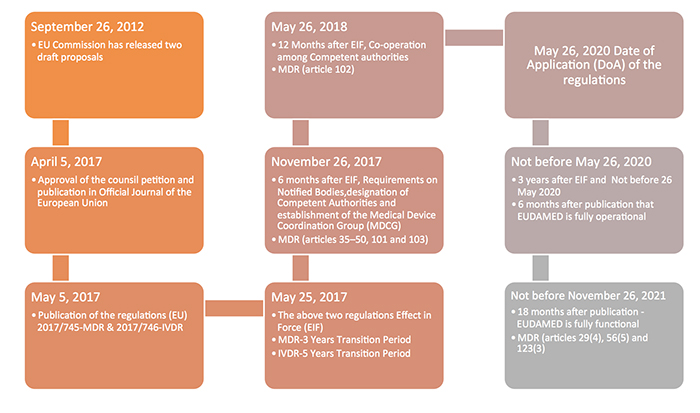
欧盟委员会于2017年5月5日发布的新欧洲(EU)医疗器械法规(MDR)修改了欧盟医疗器械指令(MDD)的主要部分,为所有器械制造商,经济运营商和指定机构提高了合规性标准。新法规显示了迈向医疗器械法规全球化的道路,通过引入独特的器械标识(UDI),一般安全和性能要求,技术文档,分类规则,合格评定程序和临床研究。

“医疗设备”一词涵盖了多种产品,从简单的温度计到用于使用患者测试报告数据诊断疾病的人工智能软件程序。随着医学和科学创新的数字化和快速发展的到来,满足用户需求的新产品的开发正以惊人的速度发展。然而,随着涉及诸如PIP乳房植入物丑闻之类的设备的严重案件的到来,需要更严格的法规。
总览
“应加强包括监管指定机构,合格评定程序,临床调查和临床评估,警惕性和市场监督在内的现行监管方法,以进一步加强。此外,应引入更多条款以确保医疗器械的透明度和可追溯性,以改善健康和安全性。” – 2017/745号法规
| 医疗器械指令 | 医疗器械法规 |
| 93/42 / EEC(MDD)-43页 90/385 / EEC(AIMD)-20页 |
法规EU 2017 / 745-177页 废除理事会指令90/385 / EEC和93/42 / EEC(MDD + AIMD) |
| 23条,十七附件 | 123条,十七附件 |
| 分类规则总数:18 | 分类规则总数:22 |
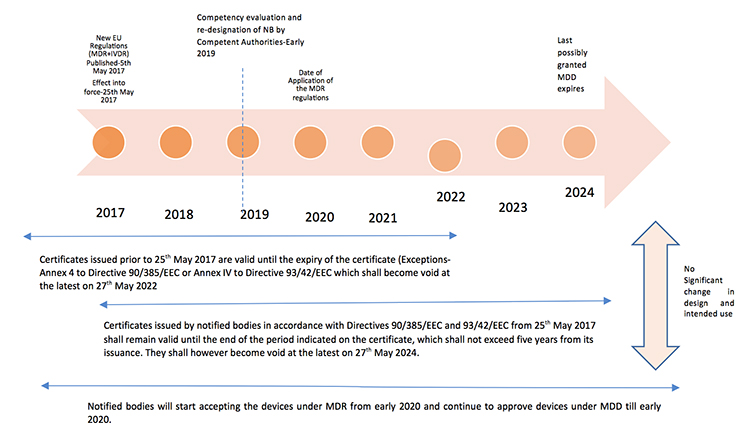
过渡时间表和证书的有效性
了解MDR
1. 考虑设备的分类;完成您的产品组合
如果您的设备当前是医疗设备的附件,具有美学目的或其他非医疗目的的产品,包含药物的临界产品,组合产品或软件产品,则应评估新的医疗设备法规用于设备的分类和上分类。
设备的分类和上分类对制造商有重大影响,因为欧盟MDR规定了更严格的合规性,安全性和功效要求。由于合规成本高昂,这将在最终确定当前和将来的产品组合中扮演关键角色。任何更改都应从管理层开始,包括决定欧洲市场产品组合,评估基于CE认证的全球产品批准和市场准入的影响的关键决策者。
在规定的时间表内不遵守新要求将导致失去在欧洲销售产品的许可。
2. 确定主要的合规要求
熟悉新的MDR术语:医疗设备协调小组(MDCG),一般安全和性能要求,通用规范,唯一设备标识,虚拟制造商。
对于根据新规则新分类为医疗器械的产品,将加强对指定机构的审查。根据重新分类和现有产品的新法规,应准备好新文档以进行CE认证。应制定的一些关键技术文件包括:
- 风险分析文件
- 临床数据可用性分析和计划
- 一般安全和性能要求
- 通用规格推导
- 所有相关的质量检查SOP
- 根据权利要求的设备性能评估测试
- 标签更新
- 符合ISO 13485产品制造和认证要求
- PMCF计划
3. 差距分析和战略最终定稿
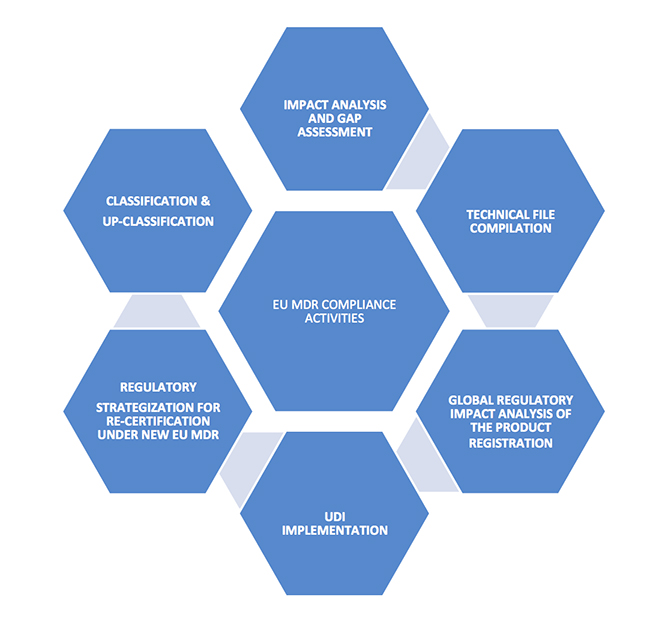
分类和上分类
- 根据新的欧盟MDR分类规则对设备进行分类和上分类
- 根据新的欧盟MDR分类规则对非医疗设备/配件进行分类
影响分析和差距评估
- 新法规对产品的总体影响评估(质量/临床/质量管理体系)
- 根据新的欧盟MDR重新认证设备的过渡计划(包括重新分类的设备)
- 根据新的欧盟MDR评估对技术文件的OEM / OBL要求进行重新认证的附加要求的标识(OEM:原始设备制造商; OBL:自有品牌标签)
技术文件汇编
- 根据新的欧盟MDR法规汇编技术文件(包括附件/非医疗/软件设备/高风险)
- 根据较高风险等级的要求修改软件的技术文件
- 对变更的基本要求的后果进行差距分析,并汇总安全性和功效摘要
新MDR下对重新认证的监管支持
- 确定新欧盟MDR认证的认证机构
- 根据新欧盟MDR认证新设备
- 根据新欧盟MDR重新认证现有设备和重新分类的设备
- 处理公告机构查询的监管策略
UDI实施
- 从提交CE证书申请书起产品权的要求
- 确定制造商的UDI代理商
- 编写应用程序的UDI要求
- UDI变更的监管策略,以将产品修改为制造商
产品注册的全球法规影响分析
- 有关重新认证对基于欧洲认证的产品注册的全球市场的影响的监管情报
- 继续保持产品活跃的全球市场注册状态的监管策略和方法
结论
尽管UDI,EUDAMED,医疗设备协调小组(MDCG),通用安全和性能要求,通用规范中不断发展的准则和新医疗器械法规的解释,但新的EU MDR仍然遵守更严格的安全性和有效性要求。与医学创新的不可思议的进步相比,这提高了监管评估和认证的标准。制造商应在研发,设计开发和扩大设计规模的早期评估这些变化的影响,以确保产品的制造和商业化符合欧盟法规。
【海外顾问帮】是协助国内企业和个人跨境发展一站式的服务中心,协同全球专家顾问,坚持透明服务,打破跨境壁垒,为医疗器械CE认证提供一站式服务,咨询电话: 400-106-2206。