医疗器械类产品对患者的安全保障尤为重要,因此就要从头抓起保证医疗器械生产到销售的每一个环节,让每一个医疗器械的消费者拥有安全有效的医疗器械,那就需要医疗器械唯一标识UDI以及美国一类医疗器械UDI组成,下面一起了解下。
医疗器械唯一识别系统由UDI代码、UDI数据载体和UDI数据库组成。
一、UDI编码
UDI是由字母和数字组成的一系列代码,分为设备标识和生产标识两部分。
设备标识码DI是静态信息,由企业标识码和产品类别码组成。它对应于GS1全球统一编码识别系统中的GTIN码,是UDI码的必要组成部分。作为医疗器械产品在供应链中的标识,可以作为“关键词”在医疗器械唯一标识数据库中搜索产品的相关信息。
生产标识码PI属于动态信息,包括医疗器械产品的生产日期、有效期、批号、产品序列号。对应GS1全球统一编码识别系统中的AI码,属于医疗器械产品的动态附加信息,是UDI码的可选组成部分。
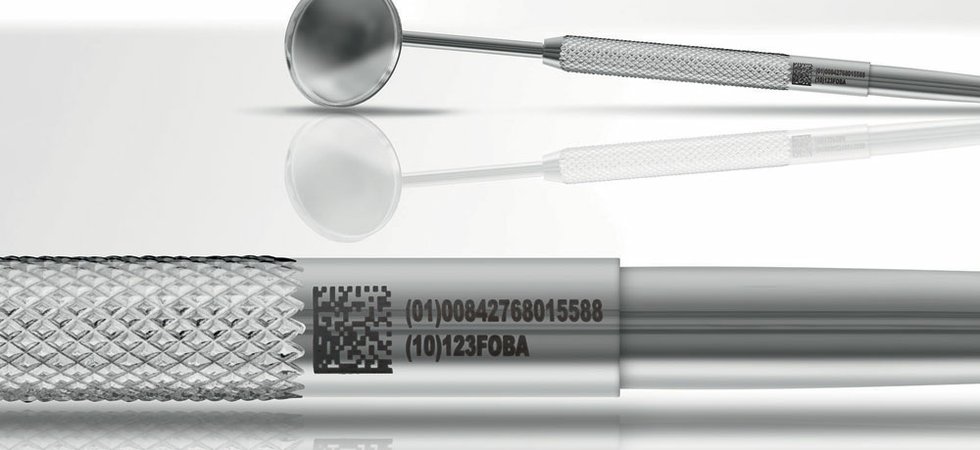
二,一类医疗器械UDI数据载体
市场上常用的UDI数据载体包括一维码、二维码和射频识别标签一维码的应用多年来已经相当成熟,可以很好的兼容市场上现有的扫码设备,成本低廉;但一维码占用空间大,纠错能力差。
二维码与一维码相比,在同一空间可以容纳更多的数据,在医疗器械包装尺寸有限的情况下可以起到非常好的作用,纠错能力强;但是对读取设备的要求比一维码高。
不同于一维码和二维码,RFID RFID标签有一个芯片,可以接收阅读器的电磁调制信号,并返回相应信号的数据载体。相比一维码和二维码,RFID的载体成本和读取设备成本要高得多,但它具有读取速度快、批量读取等优点,在一些环节和领域可以发挥特殊的作用。
三、一类医疗器械UDI数据库
医疗器械唯一标识数据库是医疗器械唯一标识系统的重要组成部分。2019年12月10日,美国食品药品监督管理局国家医疗设备唯一识别数据库正式启动。2019年12月至2020年6月,数据上报功能向试点企业开放。
医疗器械注册人/申报人应根据相关标准或规范的要求,上传、维护和更新唯一标识数据库中的相关数据。为配合SFDA医疗器械唯一标识试点工作,中国商品编码中心启动了中国商品信息服务平台与NMPA UDID对接试点工作。
四、建立UDI制度的意义
从医疗行业的角度来看,该系统的建立有利于利用信息技术手段提高医疗器械从生产销售到终端使用的准确性和一致性。
对于医疗器械生产企业来说,使用唯一标识有助于提高企业信息化管理水平,建立产品可追溯体系,强化企业满足法律法规要求的主体责任,提升企业管理效率。
UDI是医疗器械产品的电子身份证,数据载体是存储或传输医疗器械唯一标志的数据介质; 数据库是存储医疗器械唯一标识的产品标识和相关信息的数据库。在信息时代背景下,UDI是实现医疗器械产品自动识别、精确召回、跟踪跟踪、全程掌握、信息互联、智能管理的重要基本要素。
以 上就是关于”美国一类医疗器械UDI组成“的相关内容,了解更多点击咨询。














